В социологических опросах многие отвечают, что гастрит — это дискомфорт в эпигастрии и рвота, особенно тесно связанные с чрезмерным употреблением алкоголя, острой, недоброкачественной пищи, кофеина. Клиницисты считают его удобным термином, когда имеют дело практически с любым симптомом зоны эпигастрия, поскольку он дает квазинаучный ярлык, которым пациент может удовлетвориться. Патолог диагностирует заболевание по гистологическим изменениям стенки желудка: наличию воспалительных клеток, степени атрофии. Гематолог подразумевает полную атрофию, характерную пернициозной анемии.
Гастрит — воспалительный процесс в слизистой оболочке желудка, связанный с ее морфологической и функциональной перестройкой (острый), атрофическим процессом (хронический) [12].
Классификация
По Международной классификации болезней 10-го пересмотра (К29.0) выделяют два варианта гастрита: острый (К29.0-К29.2) и хронический (К29.3-К29.5), который классифицировали на:
- поверхностный;
- атрофический;
- неуточненный: антральный или фундальный [13].
Согласно Сиднейской классификации, представленной на Международном гастроэнтерологическом конгрессе в 1990 году, были пересмотрены основные критерии: морфологические, этиологические, топографические. В рамках данной системы по топографии выделили варианты следующих локализаций заболевания:
- антральная;
- фундальная;
- антрума и тела (пангастрит).
Хьюстонская классификация (1994 г.) предложила разделить нозологию на типы:
- А — аутоиммунный, атрофический;
- В — хеликобактерный неатрофический (антральный);
- В — хеликобактерный атрофический;
- С (химико-токсический, лекарственно-индуцированный и пострезекционный);
- особые формы (гранулематозный, эозинофильный, лимфоцитарный, гипертрофический) [16].
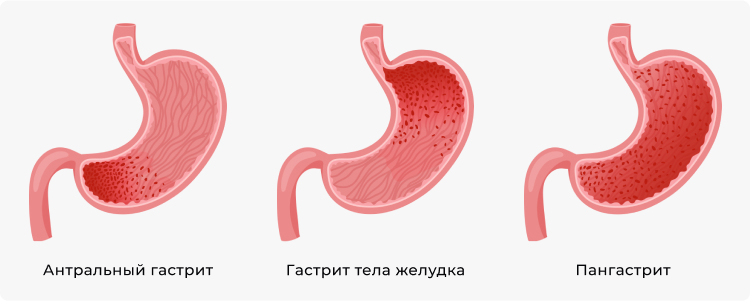
Определение понятия «антральный гастрит»
Хронический гастрит — это заболевание, характеризующееся воспалительным процессом, приводящим к атрофии эпителиальной выстилки, кишечной метаплазии, функциональным расстройствам. Занимает ведущую позицию среди всех известных заболеваний ЖКТ, составляя около 35% случаев, среди болезней желудка – 80–85% [16].
Говоря об антральном типе, учитывают его локализацию в нижнем выходном отделе, а также бактериальную этиологию (тип В, Хьюстенская классификация).
Этиология гастрита антрального отдела желудка
Первое выделение Helicobacter pylori в 1982 году Маршаллом и Уорреном открыло новую эру в микробиологии. Данные указывали на то, что данная нозология связана с развитием аденокарциномы, самой распространенной злокачественной опухоли в мире, но истинная причина тогда была неизвестна. В 1991 году в четырех сообщениях впервые была показана связь нозологии с инфекцией. В 1994 году International Agency for Research on Cancer (IARC) признало микроорганизм канцерогеном.
В настоящее время имеются обширные данные о причастности возбудителя к патогенезу хронического поверхностного гастрита (употребление бактерии двумя добровольцами привело к данному заболеванию [4, 5].
Выяснилось: наличие хеликобактериоза связано с нозологией типа В, но не с типом А, желчным рефлюксом. Затем было зарегистрировано несколько вспышек эпидемической гипохлоргидрии. На основании клинического анамнеза, гистопатологического исследования, серологических результатов доказали, что эти случаи были вызваны ятрогенной инфекцией [7].
Патогенез
H. pylori способна колонизировать и сохраняться в уникальной биологической нише. Предполагаемые патогенные детерминанты можно разделить на основные группы: вирулентные, способствующие патогенетическим эффектам, и поддерживающие, позволяющие активно колонизироваться, оставаться внутри хозяина.
Патологический процесс, характеризующийся инфильтрацией эпителия полиморфноядерными лейкоцитами, мононуклеарами, неизменно присутствует у пациентов, инфицированных H. pylori, это позволяет предположить: воспаление необходимо для выживания in vivo.
Факторы механизмов повреждения тканей:
- интерлейкин-8 (небольшой пептид (хемокин), секретируемый различными типами клеточных элементов, служащий мощным медиатором воспаления, активирующим нейтрофилы);
- фактор активации тромбоцитов;
- липополисахарид (ЛПС) (разрушает стенку органа, препятствуя взаимодействию между муцином и ее рецепторами, способствует прикреплению микроорганизма, повышенной продукции пепсиногена – агрессивного агента);
- уреаза (мощный стимулятор активации мононуклеарных фагоцитов, продукции воспалительных цитокинов, фактор колонизации, вирулентности);
- фосфолипаза (разрушает богатый фосфолипидами защитный слой на апикальной мембране клеток слизи);
- муциназа (деполимеризует защитный слизистый гель);
- вакуолизирующий цитотоксин VacA (индуцирует кислые вакуоли в цитоплазме эукариотических клеток);
- цитотоксин CagA (отвечает за ремоделирование актина, ингибирование роста, апоптоз);
- активные формы кислорода;
- индуцибельная синтаза оксида азота (связана с иммунной активацией и повреждением тканей);
- АТФ-аза Р-типа (представляет особый интерес в исследованиях, поскольку является мишенью бактерицидного действия современных препаратов, таких как лансопразол или омепразол);
- адгезины и клеточные рецепторы [2].
Механизм уклонения бактерий от иммунного распознавания
Хотя H. pylori имеет способность стимулировать иммунную систему к выработке антител, существует подавляющая активность в отношении клеточного иммунного ответа человека, опосредуемого белком [3]. Возбудитель проявляет устойчивость к уничтожению фагоцитами из-за повреждения фагосомальных мембран продуцируемым аммиаком. Экспрессия антигенов Льюиса на поверхности способствует маскировке среди антигенов эпителиальной выстилки.
Другой потенциальный механизм — изменение морфологии. Бациллярные формы превращаются в коккоидные формы после длительного культивирования. Они представляют собой устойчивую к окружающей среде покоящуюся фазу, которая может перейти в вирулентную бациллярную форму in vivo.
Клиническая картина
Тип В получил антральную локализацию, так как является основным местом колонизации. Развивающиеся изменения в этом отделе провоцируют гиперсекрецию соляной кислоты по обратной связи, ведущую к изъязвлению оболочки органа. Если процесс затягивается, то слизистая атрофируется, развивается антральный гастрит, распространяющийся на другие отделы. Зачастую он является одной из начальных стадий патологического процесса и приводит к аденокарциноме.
Сначала симптомы проявляются неярко: развиваются неатрофические изменения с клиникой, характерной для язвенной болезни (эпигастральные боли («тощаковые», проявляющиеся утром натощак/голодные/ранние (через 30–60 мин после еды)/поздние (через 90–120 мин после еды)), диспепсические расстройства, отрыжка кислым/воздухом, нарушение аппетита) [16]. Возможно местное напряжение мышц брюшной стенки и болевые ощущения в пилорической части при пальпации.
На последних стадиях пациент теряет вес.
Диагностика
С помощью гастрографии с контрастированием определяют изменения: утолщение складок, расстройство перистальтики, спазм сфинктера. На ФЭГДС видны зоны гиперемии, отечность, очаги кровоизлияний в антральном отделе. При регургитации двенадцатиперстной кишки в просвете находится дуоденальное содержимое.
В настоящее время доступны различные диагностические методики. Гистологическое исследование ткани, бактериальный посев, экспресс-тест на уреазу, использование ДНК-зондов, анализ ПЦР, используемые для исследования, включают метод эндоскопии. Дыхательные тесты, серология, ПЦР желудочного сока являются неинвазивными тестами, не требующими эндоскопии. Выбор теста в большинстве случаев будет зависеть от требуемой клинической информации, а также от доступности и стоимости отдельных тестов на местном уровне.
При эндоскопии у многих взрослых с данной патологией внутренняя поверхность желудка выглядит нормально. Распределение H. pylori и связанное с ним воспаление часто носят пятнистый характер. Очаговый характер инфекции может привести к ошибкам взятии проб эндоскопическим методом, что приведет к ложноотрицательным результатам биопсии. Два состояния, наблюдаемые непосредственно эндоскопистом, антральная узловатость и неосложненная язва двенадцатиперстной кишки, почти всегда связаны с данной инфекцией.
Метод культур имеет два основных преимущества: он позволяет тестировать чувствительность к противомикробным препаратам; изоляты, полученные культуральным путем, могут быть детально охарактеризованы. Другим эффективным методом является уреазный тест. Австралийский CLOtest, разработанный Marshall, был первым коммерчески доступным уреазным тестом, разработанным специально для обнаружения хеликобактериоза [2]. Он состоит из агарового геля, содержащего феноловый красный и мочевину; в присутствии уреазы мочевина гидролизуется, что приводит к изменению pH (цвета) индикатора. Тест интерпретируется в течение 24 часов после помещения образца биопсии на агаровый гель. Сейчас рекомендуют дыхательные ХЕЛИК-тесты с индикаторной трубкой (особенно распространен С-уреазный тест с меченной мочевиной С13), обладающие высокой эффективностью (чувствительность 94,74%, специфичность 94,44%), чтобы качественно оценить эрадикацию [11].
ПЦР — достаточно перспективный высокочувствительный метод обнаружения. Факторы, влияющие на точность теста, включают выбор праймеров, ДНК-мишени, подготовку образца, плотность бактерий. Потенциальное преимущество ПЦР заключается в том, что она позволяет поставить диагноз неинвазивно путем обнаружения ДНК в нежелудочных жидкостях (слюна). В одном исследовании чувствительность ПЦР слюны составила 84%.
Лечение
На первом этапе в период обострения пациенту назначают лечебную диету, стол №1б с дробным питанием 4–6 раз в день, в последующем переводят на стол №1. Диета при наступлении ремиссии содержит следующие ограничения: исключение сложноусваиваемой пищи (соленого, копченого, жирного), продуктов, вызывающих брожение (молочная продукция, свежая выпечка) [16].
Главной целью терапии является этиологическое направление, включающее борьбу с возбудителем. Эрадикация включает три основные линии терапии (Маастрихтское соглашение (2012 г.)).
Первая линия (10–14 дней):
- ИПП:
- Омепразол 20 мг 2 раза в день;
- Лансопразол 30 мг 2 раза в день;
- Пантопразол 40 мг 2 раза в день;
- Рабепразол 20 мг 2 раза в день;
- Эзомепразол 20 мг 2 раза в день.
- Кларитромицин 500 мг 2 раза в день.
- Амоксициллин 1000 мг 2 раза в день или Метронидазол 500 мг 2 раза в день.
Вторая линия (10–14 дней):
- ИПП
- Висмута трикалия дицитрат 120 мг 4 раза в день.
- Метронидазол 500 мг 3 раза в день.
- Тетрациклин 500 мг 4 раза в день.
Третья линия (7–дней):
- Левофлоксацин 500 мг 2 раза в день.
- ИПП.
- Амоксициллин 1000 мг 2 раза в день.
Симптоматическая терапия состоит из препаратов, снижающих кислотность (антисекреторные, антациды), снимающих спазм пилоруса (спазмолитики), нормализующих перистальтику (метаклопрамид), гастроцитопротекторы.
Физиотерапевтические процедуры также используют как репаративный метод полного выздоровления.
Профилактика
Благоприятный прогноз может быть достигнут только за счет своевременной терапии и соблюдения здорового образа жизни. В противном случае поражение принимает диффузный характер, есть риск перехода в злокачественную форму.
Вторичная профилактика — это успешная эрадикация H. pylori. Сейчас распространилось лечение «по требованию»: после первых признаков болезни пациенты принимают антациды/прокинетики/антисекреторные препараты, если двухнедельная терапия не помогла, то больные обращаются к врачу в течение 2–3 дней.

Заключение
Несмотря на то, что распространенность возбудителя снижается, антральный гастрит еще долгое время будет распространенной патологией. С учетом определенных данных об этиологии, патогенезе, течении хеликобактериоза можно предположить: заболевание не исчезнет, пока необходимый уровень гигиены, социально-экономического положения, устойчивого повышения качества жизни не будет достигнут.
Список литературы
- Croft D. N. Gastritis / Br Med J. – 1967. –28;4(5572). – р. 164-166. doi: 10.1136/bmj.4.5572.164.
- Dunn B. E., Cohen H., Blaser M.J. Helicobacter pylori / Clin Microbiol Rev. – 1997. –10(4). – р. 720-41. doi: 10.1128/CMR.10.4.720. J. Med. 324:1043-1048.
- Knipp, U., S. Birkholz, W. Kaup, and W. Opferkuch. Immune suppressive effects of Helicobacter pylori on human peripheral blood mononuclear cells / Med. Microbiol. Immunol. – 182. – 1993. – р. 63-76.
- Marshall, B. J., J. A. Armstrong, D. B. McGechie, and R. J. Glancy. Attempt to fulfill Koch's postulates for pyloric Campylobacter / Med. J. – 142. – 1985. – р. 436-439.
- Morris, A., and G. Nicholson. Ingestion of Campylobacter pyloridis causes gastritis and raised gastric pH / Am. J. Gastroenterol. – 82. – 1987. – р. 192-199.
- Owen D. A. The morphology of gastritis / Yale J Biol Med. – 1996. – 69(1). – р. 51-60.
- Peterson, W. L. Helicobacter pylori and peptic ulcer disease / N. Engl. – 1991.
- Sipponen P., Maaroos H. I. Chronic gastritis / Scand J Gastroenterol. – 2015. –50(6). – р. 657-67. doi: 10.3109/00365521.2015.1019918.
- Арутюнов, Г. П. Руководство по внутренней медицине / Г. П. Арутюнов, А. И. Мартынов, А. А. Спасский – Москва : ГЭОТАР-Медиа. – 2015. – 800 с.
- Егоренкова, Е. А. Современные методы лабораторной диагностики Helicobacter pylori / Е. А. Егоренкова, М. А. Слободина // Бюллетень Северного государственного медицинского университета. – 2022. – № 1(47). – С. 21-23.
- Лазебник, Л. Б. Использование неинвазивного дыхательного ХЕЛИК-теста в диагностике инфекции Helicobacterpylori / Л. Б. Лазебник, М. Н. Рустамов // Экспериментальная и клиническая гастроэнтерология. – 2013. – №10. – С. 38-39.
- Мухин, Н. А. Пропедевтика внутренних болезней : учебник / Мухин Н. А. , Моисеев В. С. – 2-е изд. , доп. и перераб. – Москва : ГЭОТАР-Медиа. –2015. – 848 с. – ISBN 978-5-9704-3470-3.
- Патологическая анатомия: руководство к практическим занятиям [Электронный ресурс] : интерактивное электронное учебное издание / Коган Е.А., Бехтерева И.А., Пономарев А.Б. – М. : ГЭОТАР-Медиа.
- Скворцов, В. В. Актуальные вопросы диагностикии лечения антрального гастрита типа В / В. В. Скворцов, Е. М. Скворцова // Поликлиника. – 2012. – № 1-1. – С. 102-106.
- Сторожаков, Г. И. Поликлиническая терапия : учебник. Сторожаков Г. И., Чукаева И. И., Александров А. А. 2-е изд., перераб. и доп. – 2011. – 640 с. : ил. – 640 с. – ISBN 978-5-9704-1772-0.
- Чамсутдинов Н.У. Хронический гастрит. Лекция для студентов медицинских вузов и врачей. – Махачкала: ДГМА. – 2001. – 28 с.